

Геохимия океана. Происхождение океана
Содержание
1. Океан. Как он произошел?
2. Физические свойства морской воды
3. Химический состав морской воды
4. Газы, растворенные в морской воде
5. Вариации солености и температуры океана
6. Электрохимические процессы в океане
7. Обмен двуокисью углерода между атмосферой и океаном
8. Определение палеотемператур древних морей
9. Радиоактивные элементы в морской воде и глубоководных осадках
10. Заключение
11. Литература
Не для кого не является секретом, что около трех четвертых земной поверхности покрыты водой.
По составу морская вода — водный раствор неорганического электролита. Происхождение вод мирового океана и содержащихся в них солей — один из самых интересных и интригующих вопросов.
Не оценимую услугу в установлении химического состава воды океана оказали палеонтологические исследования. Согласно данным, имеющимся в настоящее время данным, физические и химические свойства океана, по-видимому, в течение геологического времени остовались проктически не изменными. Это подтверждается тем, что биологические виды прошлого более или менее сходны с современными видами.
Геохимическое решение этой проблемы заключается в попытке сопоставления количества состава эродированных изверженных и осадочных горных пород с количеством и составом растворенных в океане солей. Одна из главных трудностей — объяснить содержание в морской воде и осадочных породах огромное количество анионов, таких как карбонатный, хлоридный и сульфатный. Эрозией изверженных пород невозможно объяснить присутствие в современном океане многих летучих, и большая часть таких элементов, как C, CI, S, N, B, Br, F и т.д., содержащихся в современном океане и связанных в осадочных породах, должна поступать из внутренних частей Земли.
Скорей всего хлор, азот, сера и фтор поступали в виде HCI, NH 3 , H 2 S и HF; углерод в виде CH 4 , CO И CO 2 , а значительная часть кислорода в виде H 2 O, СО 2 и СО.
Но как протикал этот процесс? Для ответа на этот вопрос, понадобится рассмотреть некоторые условия образования Земли.
Согласно одной из гепотез, Земля первоначально была раскаленным шаром, и поэтому могла произойти частичная потеря летучих, но и большая их часть должна была сохраниться внутри Земли. Именно эта часть летучих поступает после охлаждения на поверхность Земли в виде постепенного непрерывного потока.
Если бы летучие были утеряны в самом начале образования, то рН первичного океана должена была быть примерно 0,3. Это была бы очень сильная кислота, которая просто бы растворила большенство известных пород. Когда концентрация Са 2+ , Mg 2+ , и СО 2- 3 в водном растворе достигла точек растворения кальцита и доломита, начался процес быстрого осаждения карбонатов. Благодорая этому из первичной атмосферы и гидросферы стала быстро извлекаться углекислота, что в привело к возникновению условий, пригодных для существования живых организмов.
Рассмотрим еще один способ появления океана. Допустим, что исходное парциальное давление двуокиси углерода было ниже 1 атм и что общее атмосферное давление примерно на 10% больше современного. Тогда осаждение карбонатов должно было начаться к моменту эрозии около 240 х 10 20 г изверженных пород и по достижении рН примерно 5,7. Тогда количество избыточных летучих в гидросфере не должно быть больше 1/10 от современного их содержания из внутренних частей Земли. Одновременно с этим кислород поступал за счет жизнедеятельности первых живых организмов. Преблезительно таким путем шло формирование гидросферы, которую мы имеим сейчас.
Существует точка зрения, выраженная Калпом (1951), что гидросфера могла сформироваться постепенно за счет поступления воды из внутренних частей Земли, после остывания ее поверхности до какой-то определенной температуры. Хотя температура более глубоких зон земной коры и мантии точно не известна, но, по-видимому, он не выше 1000 о С. при столь высокой температуре Н 2 О не может входить в кристаллическую решетку каких бы то ни было минералов. Поэтому, подобно газу, газообразная Н 2 О, мигрируя сквозь породы, терялась земной корой. Однако в отличие от газа при приближении воды к земной поверхности часть ее соединялась с веществом коры и образовала гидраты: остальная часть поступала в гидросферу и атмосферу.
Расмотирим теорию появления воды из горячих источников. Принято считать, что водные пары горячих источников Йелоустонского парка содержат 10-15 % магматической воды, а горячие источники Айдахо – 2,5% ее. Но даже если бы содержание магматической воды в воде горячих источников было меньше 1%, то в течении 4,5 млрд. лет они могли бы выбросить достаточное количество воды для объяснения существования океана. По крайней мере, существование такой магматической воды поддерживает идею о том, что вода современного океана скопилась за счет постепенного поступления из внутренних частей Земли.
Теологические доказательства постепенного формирования океана.
Ревель (1955) пологал, что образование океана происходило постепенно. Он предоставил доказательства того, что значительная часть океана возникла после позднего мезозоя. Присутствие плосковершинных морских гор, коралловых атоллов и гайотов на обширных территориях так называемого “андезитного пояса” Тихого океана указывает на опускание морского дня относительно уровня моря. Этому опусканию отвечает увеличение общего объема морской воды примерно на четверть современного объема вод океана. Другие доказательства возможности опускания морского дна в течении последних 100 млн. лет были получены при палеонтологических исследованиях ископаемой фауны в керне скважин, пройденных в Тихом океане. Кроме того, это высказывание подтверждают плосковершинные морские горы между Гавайскими островами и островами Вейк, поднимающимися с глубины 5000-6000 м ниже современного уровня моря.
Ревель отмечает, что ввиду резкого расцвета в позднем мезозое пелагических фораминифер возможно было повашенное поступления двуокиси углерода из внутренних частей Земли, сопровождавшееся соответствующим увеличением поступления воды.
2. Физические свойства морской воды
Плотность.
![]() Для краткости плотность морской воды р выражается через , определяемую следующим обрзом:
Для краткости плотность морской воды р выражается через , определяемую следующим обрзом:
![]() При нормальном атмосферном давлении плотность морской воды зависит от температуры Т, солености S или хлорности CV. Взаимоотношения плотности и хлорности, при нормальных температуре и давлении выражаются формулой Кнудсена:
При нормальном атмосферном давлении плотность морской воды зависит от температуры Т, солености S или хлорности CV. Взаимоотношения плотности и хлорности, при нормальных температуре и давлении выражаются формулой Кнудсена:
В таблице 1 даны значения коэффициента расширения морской воды при давлении, равном 1 атм.
Удельная теплота.
![]() Зависимость удельной теплоты (С
р
) морской воды при 0
0
С и давлении в 1
атм
от солености может быть выражена формулой Кувахара.
Зависимость удельной теплоты (С
р
) морской воды при 0
0
С и давлении в 1
атм
от солености может быть выражена формулой Кувахара.
Где S – соленость.
Таблица 1. Коэффициент теплового расширения морской воды при различных температуре и солености.
|
Соленость, % |
Температура, о С |
|||||||
|
-2 |
0 |
5 |
10 |
15 |
20 |
25 |
30 |
|
|
0 10 20 30 35 |
-105 -65 -27 7 23 |
-67 -30 4 36 51 |
17 46 75 101 114 |
88 112 135 157 167 |
151 170 189 206 214 |
207 222 237 250 257 |
257 270 282 292 297 |
303 315 324 332 334 |
![]() Точка замерзания.
Точка замерзания.
Где к t – значение точки замерзания, Cl – величина хлорности.
р=(1,240+0,00454t)Cl
![]() Упругость паров:
Упругость паров:
Где р – осмотическое давление, р – плотность; R – газовая константа; М о – молекулярный вес воды; р – упругость паров.
L (в зависимости от хлорности морской воды CL). (Таблица 2).
Таблица 2. Электропроводность морской воды (Lх10 6 ).
|
Температура, 0 С |
Хлорность, %о |
|||
|
5 |
10 |
15 |
20 |
|
|
0 5 10 15 20 25 |
8327 9653 11019 12459 13939 15471 |
15852 18329 20906 23584 26367 29242 |
22993 26548 30231 34090 38065 42180 |
29885 34454 39167 44114 49248 54551 |
 Вязкость:
Вязкость:
Где h о – коэффициент вязкости при О 0 С; t – температура морской воды; a и b - константы, меняющиеся с изменением солености.
Поверхностное натяжение (дин/см 2 )
a =75,64-0,114t+0,0399Cl
В морской воде при 25 0 С для D-линии натрия равен:
n25D=1,332497+0,000334Cl
![]() В морской воде может быть найден по формуле:
В морской воде может быть найден по формуле:
Где I о –интенсивность монохроматического света с длиной волны у поверхности моря l , I z – длина волны света на некоторой глубине z при допущении, что падающий и проходящий лучи света перпендикулярны к поверхности воды.
3. Химический состав морской воды
Главные и малые химические компоненты морской воды. (табл. 3 и 4).
Таблица 3. Химический состав морской воды.
|
Ионы |
Химический состав соли морской воды при хлорности 19 %о (Lyman, Fleming, 1940), % |
Главные компоненты морской воды, имеющей хлорность 19%о и r 20 =1,0243 (Lyman, Fleming, 1940) |
|
|
Г/кг |
Мг х атом/л |
||
|
Na + K + Mg 2+ Ca 2+ Sr 2+ Cl - Br - So 2- 4 HCO - 3 H 3 BO 3 |
30,61 1,10 3,69 1,16 0,03 55,4 0,19 7,68 0,41 0,07 |
10,56 0,38 1,27 0,40 0,08 18,98 0,065 2,65 0,14 0,026 |
470,15 0,96 53,57 10,24 0,09 548,30 0,83 28,24 2,34 0,43 |
Таблица 4. Малые компоненты морской воды.
|
Элементы |
Содержание, Мг/л |
Элементы |
Содержание, Мг/л |
Элементы |
Содержание, Мг/л |
|
He Li N Al Si P Ar Sc Ti V Cr Mn Fe Co Ni Cu |
0,0001 0,2 0,5 0,01 3 0,07 0,6 0,00004 0,001 0,001 0,00005 0,002 0,01 0,0005 0,0005 0,003 |
Zn Ga Ge As Se Br Kr Rb Sr Y Mo Ag Cd In Sn Sb |
0,01 0,0005 <0,0001 0,003 0,004 65 0,0003 0,3 8 0,0003 0,01 0,003 0,000055 <0,02 0,003 <0,0005 |
I Xe Cs Ba La Ce W Au Hg Tl Pb Bi Rn Ra Th U |
0,04 0,0001 0,001 0,9 0,0003 0,0004 0,0001 0,000004 0,00003 <0,00001 0,003 0,0002 9,0х10 -15 3,0х10 -11 0,0007 0,002 |
Соленость и содержание хлора в морской воде.
Точно определить содержание соли в морской воде затруднительно, так как при выпаривании морской воды досуха часть бикарбоната разлагается, а часть хлорида гидролизуется, поэтому было дано следующее определение понятие “солености”:
Соленость – это общее содержание твердого остатка в 1 кг морской воды, определенного после того, как весь карбонат переведен в окись, бром и йод и замещены хлором, а органическое вещество полностью окислено.
Кнудсен приводит следующую эмпирическую зависимость между хлорностью (Cl,%) и соленостью (S,%):
S=0,03+1,8050Cl,
Где Cl – “общее количество хлора в граммах, содержащееся в 1 кг морской воды после полного замещения брома и йода хлором или хлорность – это величина в граммах на 1 кг пробы морской воды, равная цифровой величине массы в граммах “серебра атомного веса”, необходимого для осаждения галогенов в пробе морской воды весом в 0,3285233 кг.
Соленость и хлорность выражаются через вес на единицу количества (1кг) морской воды. Однако при химических исследованиях часто необходимо знать количество растворенного вещества в определенном объеме морской воды. Поэтому было введено понятие “хлористости”, как числа граммов хлорида на 1 л морской воды при 20 0 С. Величина хлористости может быть определена путем умножения величины хлорности на удельный вес морской воды при 20 0 С.
4. Газы, растворенные в морской воде.
Кислород. Растворенный в морской воде кислород заимствуется из атмосферы на контакте воды с воздухом. Он образуется также при фотосинтезе морских растений. С другой стороны, кислород потребляется при дыхании живых организмов и при окислении различных веществ моря, главным образом органического детрита.
Растворимость кислорода в морской воде зависит от температуры и солености; эта зависимость может быть выражена формулой Якобсона:
V(O 2 )= 10,062-0,2822-0,006144t 2 -0,000061t 3 -Cl(0,1073-0,003586t+0,000055t 2 ),
Где V(O2) – растворимость кислорода в 1 см 3 на 1 л морской воды при нормальных температуре и давлении в условиях равновесия воды и воздуха при нормальном давлении; Cl- хлорность; t – температура воды, о С.
Интересно, что во всех океанах существует слой с минимальным содержанием кислорода, глубина которого меняется в зависимости от географии.
Однако Ричардс и Редфилд (1955) указывают, что слои с минимальным содержанием кислорода в океане наиболее часто приурочены к поверхности одной и той же плотности - s t = 27,2 / 27,3.
Свердруп (1938) рассмотрел возможные причины равновесия между динамическим притоком и биохимическим потреблением в слое минимального содержания кислорода. Считал что, существование слоя с минимальным содержанием кислорода обусловлено главным образом биохимическим расходом кислорода и характером распределения в море органического вещества и сделал заключение, что важной причиной минимума кислородного содержания является существование в океане горизонта перерыва.
Рейкстро (1947) определял скорости расхода кислорода в пробах воды, отобранных на поверхности, в слое с минимальным содержанием кислорода и в глубоководном слое. При этом начальная температура проб в течение длительного времени поддерживалась постоянной. Он установил, что расход кислорода за два года в воде слоя с минимальным содержанием, равно как и в воде глубоководного слоя, весьма незначителен. С другой стороны, поверхностная вода после небольшого выдерживания приобрела ту же концентрацию кислорода, что и пробы воды из слоя с минимальным содержанием кислорода. Рейкстро высказал предположение, что органическое вещество в вертикальной колонне воды, по крайней мере до слоя с минимальным содержанием кислорода, поступает с ее собственной площади поверхности и этим объясняется дефицит кислорода.
Мияки и Сарухаши (1956) исследовав причины вертикальной миграции в море растворенного кислорода, пришли к выводы, что дефицит кислорода тесно связан с увеличением содержания в морской воде углекислоты и с локально протекающим окислительным разложением органического вещества.
Первое исследование изотопного состава растворенного в морской воде воздушного кислорода было проведено Рейкстро, Раддом и Доулом.
Результаты масс-спектрометрических определений показали, что между величиной отношения О 18 /О 16 и количеством кислорода, растворенного в морской воде на разной глубине, существует значительное расхождение отрицательного знака. Использовав в качестве стандарта отношение О 18 /О 16 в воздухе (0,2039%), удалось установить, что разница между процентным содержанием О 18 и таковым воздуха с глубиной постепенно возрастает, достигая максимума в +0,006% в слое с минимальным содержанием кислорода, располагающемся на глубине около 700 м. После прохождения слоя с минимальным содержанием кислорода d снова уменьшается, падая на глубине 2870 м примерно до +0,001%. Доул (1952) установил, что кислород, освобождающийся при фотосинтезе, имеет более низкую величину отношения О 18 /О 16 , чем атмосферный кислород; по его данным, фактор фракционирования равен 0,983. Это должно приводить к уменьшению относительного количества О 18 в растворенном в морской воде кислороде, так как этот кислород частично производится фитопланктоном.
С другой стороны, кислород в морской воде поглощается при дыхании живых организмов, при бактериальных процессах, при окислении органического детрита и т.д.; при этом легкий изотоп кислорода поглощается избирательно. Вследствие этого следует ожидать, что находящийся в воде остаточный кислород по сравнению с воздухом должен быть относительно обогащен О 18 . По данным определений Доула (1954), фактор фракционирования изотопов кислорода при процессах поглощения кислорода, растворенного в морской воде, равен 0,991. Необходимо отметить, что азот в газе, растворенном в воде океана, так же как и атмосферный азот, имеет нормальный изотопный состав.
Азот и редкие газы. Растворимость азота в морской воде описывается следующей формулой Фокса:
V(N 2 )=18,639-0,4304t / 0,00745t 2 -0,0000549t 3 -Cl(0,2172-0,00718t+0,0000952t 2 ).
Результаты определений показывают, что содержание растворенного азота, а также аргона, неона и гелия, в отличие от кислорода мало изменяется с глубиной и всегда близко к насыщению.
В таблице 5 приведен пример данных о вертикальных вариациях содержания растворенных в воде неона и гелия в Атлантическом океане.
Таблица 5. Вариации содержания в морской воде растворенных неона и гелия (Rakestraw и др., 1939).
|
Атлантический океан (35 о 55’ с.ш. и 67 о 39’ з.д.), апрель |
|||
|
Глубина, м |
Температура, оС |
Содержание кислорода, см 3 /л |
Содержание He+Ne 10-5 см 3 /л |
|
0 5 25 62 166 333 622 912 1772 2959 |
18,28 18,31 17,97 17,93 17,92 17,63 15,62 9,55 3,86 3,16 |
5,14 5,15 5,05 5,17 5,15 4,90 4,10 3,60 5,88 6,15 |
18,5 14,1 15,2 15,2 15,2 15,6 15,9 15,9 16,5 17,8 |
5. Вариации солености и температуры океана
Вертикальная структура океана . Океан может рассматриваться как двухслойная система. Верхний слой, достигающий мощности от десяти до первых сотен метров ниже водного уровня, испытывает перемешивание и внутри него как температура, так и соленость воды в вертикальном направлении проявляют гомогенное распределение.
В расположенном ниже слое, мощность которого от поверхности раздела с верхним слоем до дна достигает нескольких тысяч метров, температура с глубиной убывает. Вертикальные вариации солености в разных местах различны, тем не менее плотность с глубиной всегда возрастает, вследствие чего вода отчетливо расслоена как результат вертикальной стабильности в слое.
В соответствии с этим в нижнем слое скорость горизонтального смешивания весьма значительна, а вертикальное перемешивание совершается медленно.
В целом, соленость выше в теплых течениях и ниже в холодных.
Латеральные вариации температуры в поверхностей зоне моря. Наиболее высокие температуры поверхности моря наблюдаются несколько к северу от экватора, где также наиболее высокая температура воздуха.
6. Электрохимические процессы в океане
Поскольку морская вода представляет собой электролит, то естественно, что в океане протекают разнообразные электрохимические процессы.
Морская вода является проводником электричества, поэтому при ее движении через магнитное поле Земли в соответствии с законом электроиндукции возникает э.д.с.
Зависимость между разницей потенциалов и скоростью течения воды в океане имеет следующий вид:
С 2j = H rot u ,
где Н – интенсивность магнитного поля Земли; u -скорость течения; j - разница потенциалов.
Электрические токи в океане, вызванные совместным действием земного магнетизма и движения воды, могут влиять на многие подводные вопросы. Например, подводный кабель, проложенный по дну узкого пролива с сильными приливно-отливными течениями, будет очень быстро корродироваться. В настоящее время получено подтверждение предположения автора о том, что коррозия начинается под воздействием электрического тока, изменяющегося в зависимости от приливного течения; коррозия ускоряется под воздействием вторичной поляризации, возникающей на корродированной поверхности кабеля.
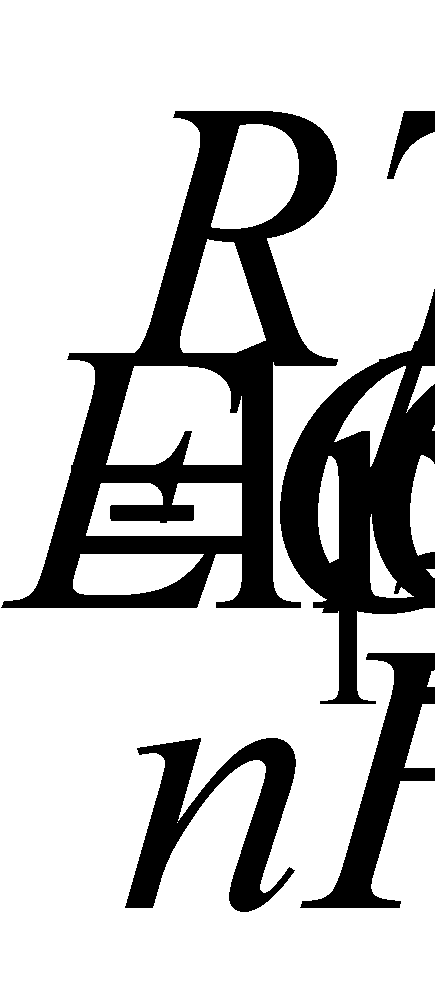 Другое электрохимическое явление океана заключается в возникновении концентрационных ячеек. Разность потенциалов
Е
определяется по формуле:
Другое электрохимическое явление океана заключается в возникновении концентрационных ячеек. Разность потенциалов
Е
определяется по формуле:
Где С 1 и С 2 – концентрации известных ионов. В открытом океане величина отношения С 1 /С 2 близка к 1, и поэтому здесь трудно ожидать возникновения большой разницы потенциалов.
Более того, ввиду присутствия в воде растворенного кислорода, часто обладающего значительным градиентом концентрации, наблюдается значительный окислительно-восстановительный потенциал. Если на борту корабля поместить каломелевый полуэлемент, а в воду погрузить платиновый электрод, то можно легко измерить разность потенциалов между электродами, изменяющуюся с глубиной в зависимости от содержания кислорода.
Номура (1941) установил, что в мелководной зоне моря между придонным и верхним слоями воды может возникать значительная разность потенциалов, достигающая иногда 0,4 в . в пресной и солоноватой воде, когда буферные реакции слабы, окислительно-восстановительный потенциал близок величине рН.
Гольдберг (1954) считает, что в основе образования марганцевых конкреций, встречаемых в глубоководной зоне лежит электрохимический процесс аккумуляции марганца и железа.
Последние исследования глубоководной зоны установили, что морская вода испытывает перемещения даже близ самого дна. Вследствие этого верхняя часть дна океана будет служить электродом. Если подводные перемещения воды связывать с приливными движениями, то дно – электрод должно попеременно приобретать разную полярность. Соли окиси марганца в морской воде, имеющие отрицательный заряд, будут осаждаться вследствие электрофореза при положительном заряде электрода, а железо бдут осаждаться при приобретении электродом отрицательного заряда. Если полярность электрода изменяется через одинаково равные промежутки времени, то в конкрециях будет аккумулироваться равное количество железа и марганца.
7. Обмен двуокисью углерода между атмосферой и океаном
Атмосферный воздух в среднем содержит 0,03 об % углекислоты. Общее содержание двуокиси углерода в атмосфере оценивается в 0,0233 х 10 20 г. В океане двуокись углерода присутствует в виде Н 2 СО 3 , НСО - 3 , СО 2- 3 , органического вещества; общее ее содержание оценивается в 1,4 х 10 20 г, что примерно в 60 раз превосходит ее количество в атмосфере.
По расчетным данным наибольшее количество углекислоты производится живыми организмами, в то же время предполагается, что количество углекислоты, расходующееся при эрозии и седиментации, сопровождаемых преобразованием силикатов в карбонаты, приблизительно равно ее количеству, поступающему за счет вулканической деятельности, деятельности фумарол, горячих источников и т.п.
Количество углерода, содержащегося в организмах, будучи выражено через СО 2 , составляет около 0,145 х 10 20 г, что в 6 или 7 раз превышает содержание СО 2 в атмосфере. Как указывал В.И. Вернадский, организмы являются важным звеном в геохимическом цикле углерода.
Другой важный момент заключается в том, что в океане в растворенном состоянии также находится колоссальное количество углекислоты. Средняя общая концентрация СО 2 в морской воде составляет 2,3 миллимоля/л. У поверхности моря, где вода соприкасается с воздухом, наблюдается тенденция к установлению одинакового парциального давления СО 2 в атмосфере и в морской воде. Таким образом, океаном может контролироваться содержание СО 2 в атмосфере. Эта идея впервые была высказана Шлезингом еще в XIX столетии.
Как будет сказано ниже, скорость обмена молекулами углекислоты между морской водой и атмосферой может быть легко установлена на основании имеющихся определений радиоуглеродного возраста морских осадков и организмов.
Величина отношения С 13 /С 12 в морских карбонатах примерно на 2,5% выше этой величины у наземной флоры. Соответственно фактор обогащения С 14 в них два раза больше, чем фактор обогащения С 13. С учетом влияния эффекта изотопного фракционирования концентрация С 14 в морских материалах, пониженная относительно его концентрации в стандартах, должна быть целиком отнесена за счет радиоактивного распада, по которому может быть определен абсолютный возраст вещества.
Крэг (1954) установил, что хотя ожидаемая величина обогащения современных морских раковин С14 равна 5%; что соответствует 400 годам абсолютного возраста углерода в поверхностных водах океана. Крэг высказал предположение, что это, возможно, результат медленного обмена двуокисью углерода, между океаном и атмосферой.
По данным Зюсса (1954, 1955), средний радиоуглеродный возраст морских организмов (по пробам из Атлантического океана) составляет 430 лет.
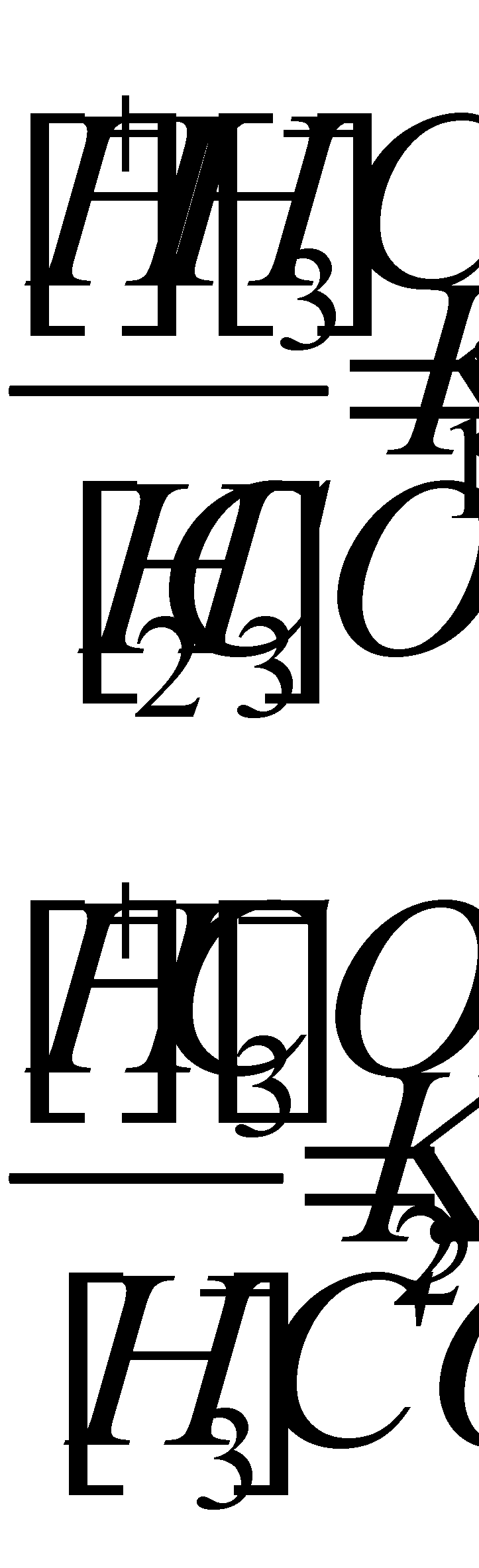 Распределение двуокиси углерода в океане
. В свежей воде угольная кислота диссоциирует следующим образом:
Распределение двуокиси углерода в океане
. В свежей воде угольная кислота диссоциирует следующим образом:
Где К1 и К2 – соответственно первая и вторая константы дисоциации, величина которых изменяется в зависимости от температуры, солености и хлорности воды. При 20 о С К 1 =4,15 х 10 -7 , р К 1 =6,38 и К 2 = 4,20 х 10 -11 , р К 2 =10,38.
Скорость обмена двуокиси углерода между атмосферой и океаном. В связи с возможным накоплением двуокиси углерода в результате сжигания больших количеств ископаемого топлива значительное внимание уделяется вопросам о распределении углекислоты на Земле в целом и о скорости обмена двуокисью углерода между воздухом и морской водой. Если количество атмосферной двуокиси углерода действительно увеличивается, то должно происходить и повышение температуры воздуха, обусловленное абсорбцией инфракрасного излучения, что должно повлечь за собой существенные изменения в климате Земли. Такая возможность в значительной степени будет зависеть от скорость обмена углекислотой между атмосферой и гидросферой.
Исходя из наблюдений за поведением С 14 в атмосфере и океане Ревель и Зюсс (1957) оценивают время пребывания углекислоты в атмосфере 14-30 лет.
Определение парционального давления углекислоты в воздухе и в поверхностных водах Атлантического океана Такахаши (1959) установили, что концентрация двуокиси углерода в воздухе непосредственно над поверхностью моря довольно постоянна, в среднем около 317,4 ррm, и что океан абсорбирует углекислоту всей площадью своей поверхности. По данным Такахаши, средняя концентрация углекислоты в атмосферном воздухе 320,8 ррm.
8. Определение палеотемператур древних морей.
Шкала палеотемператур по соотношению изотопов кислорода в органическом кальците.
Юри и его сотрудники (1951) предложили интересный метод определения температур древних морей, основанный на зависимости изотопного состава кислорода воды и карбонатных ионов от температуры. В проводившихся ими исследованиях определялось процентное содержание тяжелого изотопа О 18 в материале карбонатных ископаемых останков древних морей, которые образовались за счет отмирания обитавших в них живых организмов.
По данным Сиборга и Перльмана (1948) изотопы кислорода имеют следующую относительную распространенность: О 16 – 99,757, О 17 – 0,039, О 18 – 0,204. Величины эти могут не значительно отличатся, отклоняясь максимум на 4%.
Механизм изотпоного фракционирования при равновесном обмене был исследован Юри и Грифом (1935), Юри (1947) и другими исследователями. Значительное количество данных получено относительно обмена дейтерия и протия.
Для реакции обмена изотопов кислорода между карбонатными ионами (СО 2- 3 ) и молекулами воды (Н 2 О) фактор фракционирования может быть определен по уравнению:
![]()
![]() Где величина a приблизительно равна константе равновесия К следующей реакции обмена:
Где величина a приблизительно равна константе равновесия К следующей реакции обмена:
(1.18)
Таким образом, рассчитав К для реакции 1,17 можно получить фактор фракционирования a и его вариации в зависимости от температуры.
Фракционирование протекает более эффективно при низких температурах и величина фактора фракционирования от 0 до 25 о С изменяется на 0,44%, т.е. 0,176% на 1 о С. Поэтому определяя концентрацию О 18 , можно узнать температуру воды.
Путем определения содержания О 18 в раковинах морских животных, живущих при известной температуре, Эпштейн, Бухсбаум, Лоуенстем и Юри (1953) установили следующие зависимость между температурой и девиациями содержания О 18 .
t=16,5-4,3d +0,14d 2 ,
![]() d - в уравнении 1.18. определяется по формуле:
d - в уравнении 1.18. определяется по формуле:
где R – отношение числа молекул С 16 О 18 О к числу молекул С 16 О 2 в пробе и стандарте. В качестве стандарта карбоната использовался белемнит из формации Пиди.
Относительное содержание в морской воде О 18 . Для точного определения температуры по кислородной шкале необходимо знать соленость воды, так как относительное содержание О 18 в морской воде сильно варьирует в зависимости от ее солености. Поскольку давление водяных паров, состоящих из Н 2 О 16 на 0,8 и 1,1%, выше такового Н 2 О 18 при 25 и 0 о С соответственно, то содержание О 18 в воде океанов должно существенно зависеть от процессов испарения и конденсации.
Энштейн и Майеда (1953) определяли содержание О 18 на 93 пробах морской воды и 7 пробах пресной воды. У поверхностных вод океана девиация содержания О 18 варьирует примерно от –3,3 до 3,5%о. Средняя величина d для морской воды с глубины от 500 до 2000 м со средней соленостью 34,7%о оказалась (-0,04)-(+0,1)%о. Пониженная величина отношения О 18 /О 16 наблюдается в поверхностных морских водах, для которых возможна контаминация талых вод льдов. С другой стороны, в морской воде, разбавленной водой иного происхождения, чем вода, возникающая при таянии льда и снега, дефицит О 18 меньше, так как пресная вода, возникающая при таянии снега, имеет существенно пониженное содержание О 18 . Поэтому морская вода примерно одинаковой солености может проявлять различное относительное содержание О 18 . Интересно, что морская вода с глубин более 1000 м при той же солености содержит меньшее количество О 18 .
В таблице 6 приведены данные Эмилиани (1965) о среднем изотопном составе кислорода гидросферы.
Таблица 6. Изотопный состав кислорода гидросферы d , %о.
|
Гидросфера |
Занимаемый объем в виде Н 2 О при нормальных температуре и давлении, 10 6 км 3 |
Средний изотопный состав кислорода d , %о |
|
Океан Лед (r ср =0,88) Пресная вода Водяные пары |
1360,0 16,5 0,5 0,01 |
0 -25 -7 (-7)-(-16) |
Палеотемпературы морей. Описанным выше методом Юри и его сотрудники (1951), используя в качестве проб белемниты, попытались определить палеотемпературы морской воды верхнемелового периода.
9. Радиоактивные элементы в морской воде и глубоководных осадках.
Высокая концентрация радия в глубоководных осадках впервые была установлена Джоли (1908), который провел определения содержания радия в пробах донных осадков, собранных экспедицией Челленджера. С тех пор уже накоплено значительное количество данных о концентрации радия в глубоководных осадках. Подтвердилось также то, что морские донные осадки с глубин более 2000м обычно содержат радия больше, чем гранитоидные породы суши. Повышенная концентрация радия особенно заметна в красных глинах. (Табл.7).
Таблица 7. Содержание радия в континентальных породах и морских донных осадках, 10-12 г Ra/л
|
Континентальные породы |
Глубоководные осадки |
||
|
Граниты Базальты Осадочные породы |
0,2-0,5 0,1-1,0 0,05-0,5 |
Красная глина Глобигериновый ил Голубая грязь |
3-22 3-7 1-3 |
По данным из таблицы 7 наибольшее содержание радия среди континентальных пород наблюдается в гранитах; однако глубоководные осадки содержат радия в несколько раз больше. Что касается механизма концентрации радия в глубоководных осадках, то, согласно имеющемуся объяснению, ионий, являющийся изотопом тория и родителем радия, осаждается в них вместе с гидроокисью железа. Частично концентрация радия может быть связана с аккумуляцией в осадках самого радия; вместе с тем считается, что осаждение урана из морской воды значительно меньше.
Имеется ряд аналитических данных о содержании радия в морской воде.
Эванс и другие (1938) провели определение среднего содержания радия в сложной пробе морской воды и установили, что оно равно 0,08 х 10 -12 г/л, а среднее содержание урана в морской воде составляет 1,5 х 10 -6 г\л.
Хамагуши (1939) высказал предположение (в отношении аккумуляции радия в глубоководных осадках), что радий осаждается вместе с коллоидальными частицами гидроокиси и окиси железа и марганца. Его предположение подтверждается концентрацией марганца и железа в глубоководных осадках.
Длительность периода со времени начала генерации ионием радия до времени образования максимального количества радия по расчетам составляет около 10 000 лет.
Крел утверждает что, на распределение радия в осадках в основном влияют колебания в скорости осаждения иония, вариации общей скорости седиментации, а также диффузия и адсорбция в осадках радия и иония. Крель получил примерную величину скорости осаждения иония около 1-20 мм/1000 лет, а содержание иония в океане составляет (3,1/1) х 10 -15 г/мл.
Холланд и Калп (1956) изучали катионный обмен радия и иония на поверхности пелагических осадков, используя для иония (Th 230 ) и радия (Ra 236 ) в качестве трассеров радиоторий (Th 238 ) и торий-Х (Ra 224 ). Результаты полученные в ходу иследования показали, что количества абсорбированного осадками иония и радия сопоставимо с наблюдаемым в современных глубоководных осадках. Это свидетельствует о том, что одними из механизмов извлечения иония и радия из воды океана являются адсорбция и базовый обмен.
Аррениус, Брамле и Пиччиотто (1957) изучили распределение a -активности в глубоководных осадках севера экваториальной части Тихого океана. Полученные ими результаты свидетельствуют о том, что около половины a -активности связано с фрагментами и обломками скелетных костей рыб, экскрементами животных зоны бентоса и мелкими (,1 мк) высокопреломляющими кристаллами (вероятно, барит); другая половина, внутри пор осадков. Пятна с высокой a -активностью, наблюдаемые у обломков костей рыб, обычно связываются с изотопами тория и их производными.
Пиччиотто и Вилгейм (1954) предложили новый хронологический метод, основывающийся на отношении иония и тория (Th 230 /Th 232 ). Так как ионий или Th 230 ,имеет период полураспада гораздо больше (1,4 х 10 10 лет), то можно определить абсолютный возраст, если в пробе глубоководного осадка не содержится детритовый материал. По их данным содержание иония в морской воде менее 2 х 10 -13 г Io/л.
Самая интересная интересная проблема баланс гидросферы и атмосферы по содержанию в них СО 2 :
|
|
Содержание СО 2 , 10 20 г |
|
|
Атмосфера Океан и проточные воды Живые организмы и неразложившееся органическое вещество Осадочные породы (включая интерстиционную воду): Карбонаты Органический углерод Уголь и нефть |
0,0233 1,30 0,145 670 250 0,27 |
1,47
920 |
Из данных указанных выше видно что, углерод, некогда находившийся в первичных гидросфере и атмосфере, в настоящее время связан в осадочных породах, и количество его примерно в 600 раз превосходит содержание углерода в современных атмосфере и океане.
Предположем что, если бы всего 1% углерода существующих осадочных пород передет обратно в гидросферу и атмосферу, большенство современныех морскиех организмов перестали бы существовать.
Судя по скорости современного осадконакопления, не будь постоянного поступления новых количеств СО 2 , в гидросфере и атмосфере через несколько сотен лет наступила бы нехватка углекислоты. В этом случае вместо кальцита (СаСО 3 ) главным компонентом морских осадков стал бы брусит Mg(OH) 2 . Однако в геологической истории прошлого отсутствуют признаки резкого вымирания большого количества морских организмов или осаждения Mg(OH) 2. Поэтому весьма вероятно, что в течение всех геологических периодов баланс компонентов гидросферы и атмосферы был в значительной степени сходен с современными обуславливался постоянным регулярным поступлением СО 2 без резких колебаний его содержания.